作为2017年度癌症治疗领域的当红花旦,现如今的CAR-T细胞疗法可谓是人尽皆知。但针对移植排斥以及一系列自身免疫性疾病的CAR-Treg细胞疗法,恐怕很多人还是很陌生。
CAR-T/Treg
我国每年有100多万需要器官移植患者,其中30万左右的病人不做器官移植手术就有可能性命不保。但接受器官移植后,患者仍会面临排斥反应的巨大风险。例如,在肺移植中,手术后五年的死亡率高达40%至55%。而且相关研究表明,接受过器官移植的人群总体癌症死亡风险是普通人群的2.84倍,这很可能与为了促使移植器官被接受而使用有效的免疫抑制剂有很大关系。
另外,自身免疫性疾病的危害,更是不言而喻的,从很多方面来说,甚至不亚于癌症带来的打击。近年来,虽然该领域药物的研发可谓取得了长足的进步,但与此同步带来的不良反应多(如激素,免疫抑制剂)、费用贵、无法根治等问题,也如鲠在喉!
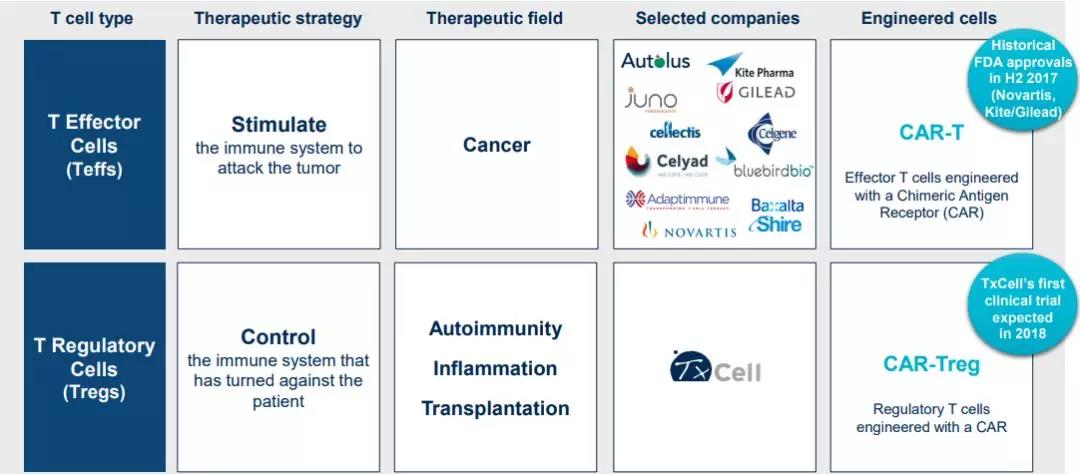
CAR-T治疗领域群雄割据
由此可见,移植排斥以及诸多自身免疫性疾病仍面临着未满足的医疗需求。于是,在CAR-T治疗领域群雄割据的今日,蛰伏于欧洲一隅的一家小企业看准市场,也开始了上演寒巢迎金凤的好戏。
开发针对自身免疫性疾病的CAR-Treg

SOT-实体器官移植、LN-系统性红斑狼疮、BP-天疱疮、MS-多发性硬化症
完成专有CAR-Treg技术生产过程开发
当地时间2017年12月18日,该公司宣布已完成其专有CAR-Treg技术的第一代生产过程的开发,而且这个过程将在首次临床试验开始之前转移到合同生产组织(CMO)。
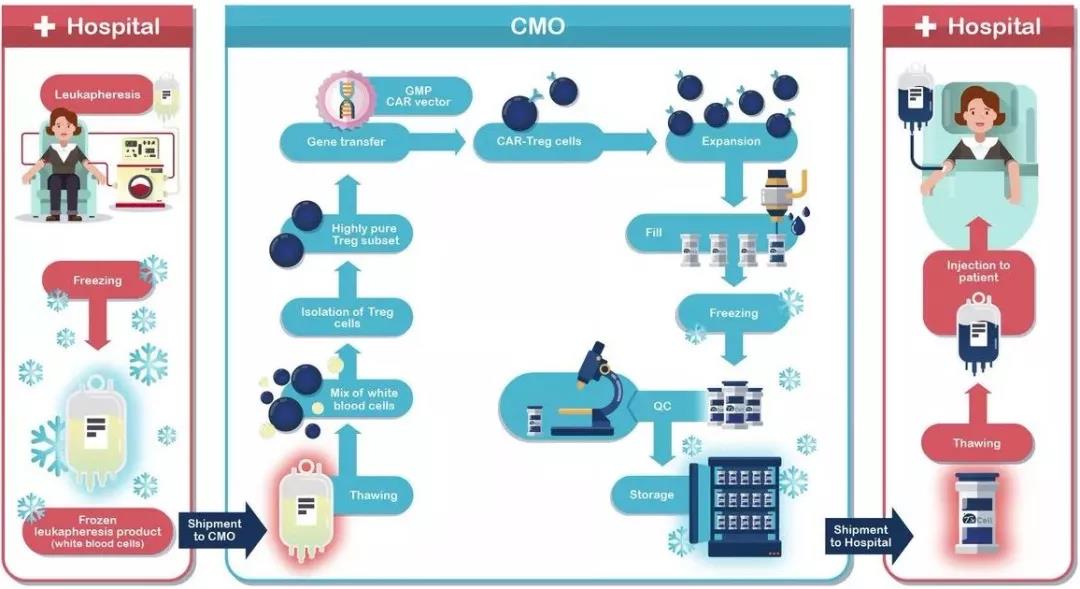
CAR-Treg生产过程
对于其第一个CAR-Treg生产过程,TxCell已经分离出一部分稳定并显示出强烈的抗炎活性的Treg细胞。尽管所筛选的Treg子集很少见,但TxCell已经在两周内(后期生产质量控制之前)成功生产了CAR-Treg细胞产品。并将于2018年2月20 - 22日在英国伦敦举行的CAR TCR高峰论坛上介绍有关该制造工艺的更多细节。
目前,TxCell公司正在完成对其首选HLA-A2 CAR Treg产品临床供应的CMO(合同生产组织)的选择。一旦执行CMO合同协议,TxCell制造过程的转移将会立即进行。预计将于2018年第四季度提交启动首次临床试验的监管档案。
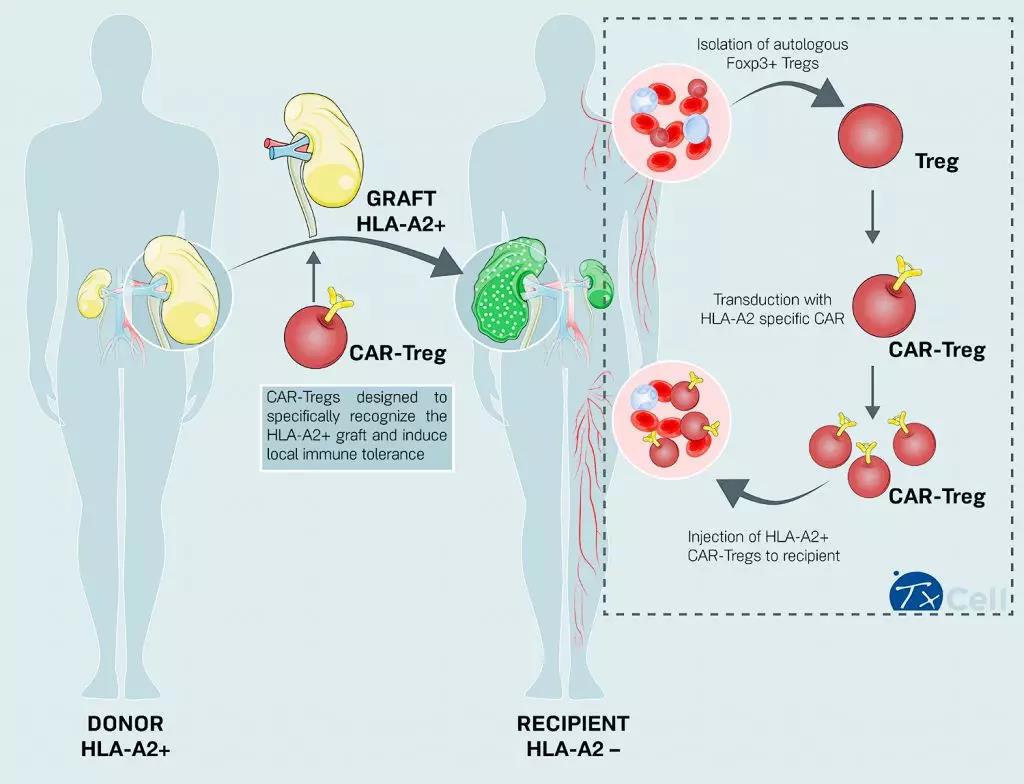
HLA-A2 CAR Treg
对此,TxCell首席执行官Stéphane Boissel表示:“在预期的时间范围内完成第一个临床候选产品CAR-Treg(器官移植,预防移植排斥反应)的生产过程对公司来说非常重要,这将使我们能够在首例患者研究中尽快评估TxCell技术平台的潜力。众所周知,接受器官移植后,患者会面临排斥反应的巨大风险,而我们提供的这款个性化细胞疗法(HLA-A2 CAR Treg)可以为预防移植器官的慢性排斥反应提供替代疗法。”
此外,TxCell为HLA-A2 CAR-Treg候选产品开发的CAR-Treg制造过程同样适用于公司的CD4+ FoxP3+ Treg产品。而且在2017年6月,TxCell已经委任了Lentigen Technology,Inc.(LTI)作为其合同生产组织(CMO),用于其CAR-Treg候选产品的慢病毒载体的GMP生产。
综上所述,TxCell公司凭借着坚实的Treg研究基础,专注研究有自身特色的CAR-Treg细胞疗法,其未来前景以及对CAR研究领域的贡献都是值得期待的。
关于HLA-A2 CAR-Treg
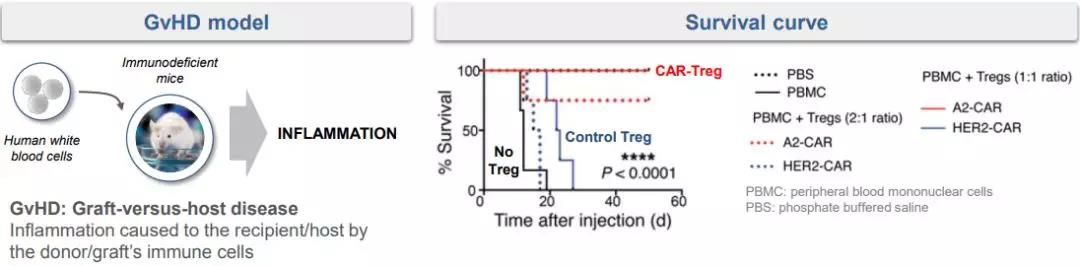
临床前研究结果
HLA-A2 CAR-Treg是TxCell公司的CAR Treg明星候选产品,它基于CD4+ FoxP3 + Treg的一个子集,靶向移植中常见的错配抗原HLA A2,正在开发用于预防器官移植后的慢性排斥反应。目前,HLA-A2 CAR Treg已经在临床前GvHD模型中显示出了强有效性,相关临床试验正在准备阶段。


